Митохондрии: как позаботиться о них и о своем здоровье?
Крошечные структуры внутри наших клеток связаны с болезнями сердца, старением и депрессией. Вот все, что нужно об этом знать
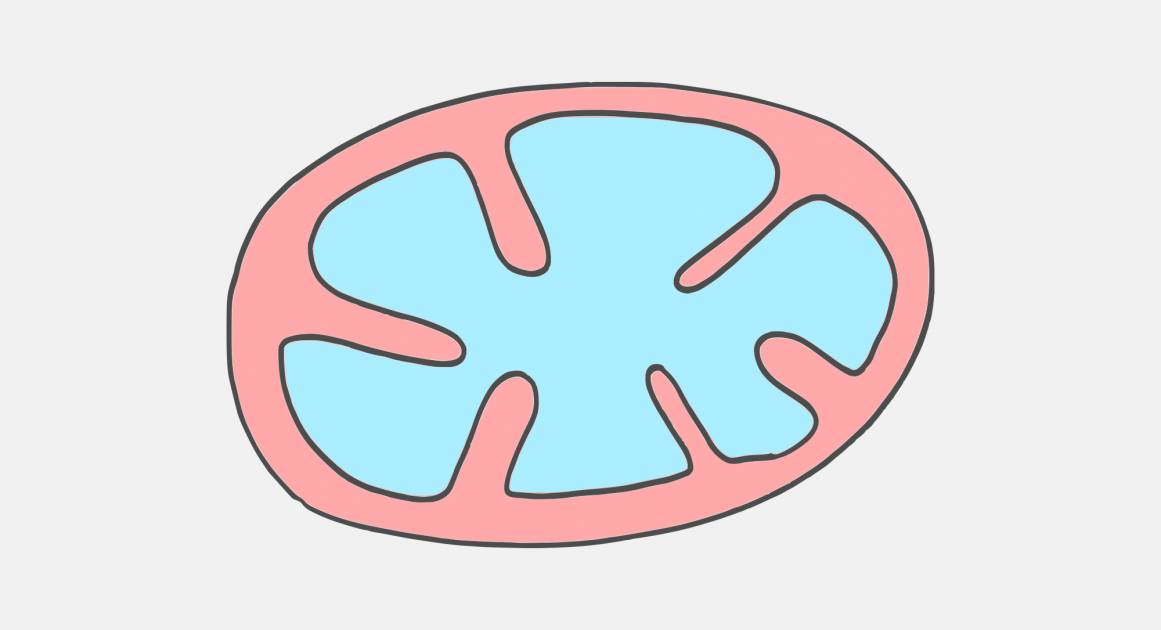
Bionet / Wikimedia / (CC BY-SA 4.0)
Примерно 2,5 млрд лет назад на Земле была заключена эпохальная сделка. Как гласит теория симбиогенеза, одноклеточные организмы, тогда еще не умевшие использовать кислород для жизни, приняли в себя бактерии, которые обладали этим ценным навыком, и так обзавелись собственными мини-фабриками по быстрому производству энергии.
Результат этой успешной бизнес-стратегии — наши митохондрии. Хоть эти крошечные органеллы (уменьшительное от «органа») давно живут внутри клеток, занимая около 25% их объема, они, похоже, не забыли о том, что когда-то были бактериями — у них, например, есть собственная ДНК. Стоит помнить об этом и нам, чтобы знать их слабые места и обеспечивать им правильное техобслуживание.
А это важно, потому что митохондрии выполняют много ключевых функций — от снабжения организма энергией до регулирования иммунитета. Именно проблемы с митохондриями многие ученые считают основной причиной старения и развития рака, сердечно-сосудистых заболеваний, диабета и болезней Паркинсона и Альцгеймера. Даже ментальные нарушения, возможно, связаны со сбоями в их работе.
Митохондрии и старение
Главная задача митохондрий — обеспечить организм энергией. Любой фабрике для производства нужно не только оборудование, но и сырье. Для митохондрий это сырье — глюкоза и жиры, которые мы получаем с пищей, и кислород, который мы вдыхаем: митохондрии используют 80% его объема из каждого вдоха.
Клетка перерабатывает сырье (глюкозу и жиры) в понятные для митохондрии метаболиты. Их митохондрия прогоняет с помощью кислорода через восемь последовательных реакций (они называются циклом Кребса) и превращает в топливо для наших клеток — АТФ. Задача этой молекулы — легко распадаться, выделяя максимум энергии, которую клетки направляют на строительные нужды. Синтез белков, запасание углеводов и жиров в организме и просто поддержание жизни — для всего этого нужно много АТФ. Впрочем, абсолютное количество этого вещества в организме не так велико — всего около 60 г, но АТФ постоянно распадается и воссоздается, и общий суточный оборот его примерно равен массе вашего тела.
Ни один механизм не совершенен. Наши внутриклеточные фабрики по производству АТФ — тоже. Когда митохондрия превращает глюкозу и кислород в энергию, образуется побочный продукт — активные формы кислорода. Они нестабильны и могут участвовать в совершенно ненужных реакциях, повреждая при этом клеточные структуры. Их влияние должны компенсировать антиоксиданты — активные формы азота или специальные белки. Они реагируют с активными формами кислорода и превращают их в безопасные соединения.
В идеале активные формы кислорода и антиоксиданты — в состоянии баланса. Тогда активные формы кислорода приносят пользу: контролируют рождение, жизнь и смерть клеток, защищают от бактерий. Если их слишком много, возникает окислительный стресс: так повреждаются биомолекулы, которым не повезло оказаться поблизости. А ближе всего — митохондриальная ДНК, которая несет информацию о белках, участвующих в производстве АТФ. Активные формы кислорода повреждают ее, и в геноме митохондрий появляются мутации. А так как митохондрии размножаются делением, как и бактерии, то эти дефекты тиражируются. И многие ученые считают, что старение — как раз результат накопления таких мутаций.
Вот как, например, описан механизм старения в потрясающем исследовании, опубликованном в Nature. Ученые создали генетически измененных мышей, клетки которых синтезировали и использовали дефектный рабочий белок. Обычно этот белок копирует митохондриальную ДНК перед тем, как митохондрия делится. Но дефектный белок при копировании не повторял ДНК дословно, а вносил случайные ошибки. В результате митохондриальные мутации у мышей накапливались быстрее, чем у обычных. При рождении и в раннем подростковом возрасте мыши-мутанты развивались нормально, но потом быстро приобретали старческие недуги: худели, теряли подкожный жир и лысели, у них развивались кифоз, остеопороз и анемия, фертильность снижалась, а сердце аномально увеличивалось. Такие мыши жили недолго.
Митохондрии и мозг
Основной потребитель энергии митохондрий — мозг: ему нужно в 10 раз больше кислорода и глюкозы, чем другим тканям. Потому дисфункция митохондрий еще и приводит к гибели нейронов, а гибель нейронов — к нейродегенерации и болезням Альцгеймера и Паркинсона, предполагают ученые.
Чтобы понять, как дисфункция митохондрий связана с болезнью Паркинсона, исследователи из Великобритании и Германии проанализировали состояние митохондрий и мозга здоровых пожилых людей и пожилых с болезнью Паркинсона. Сначала они взяли образцы мозга, тонко порезали и опустили в специальный краситель. Этот краситель связывается с одним из белков, который митохондрии используют для синтеза АТФ, — цитохромом С. Потом отмыли ткани мозга. Нейроны покрасились, но особенным образом: чем ярче окрас, тем больше цитохрома С в нейроне и тем здоровее митохондрии.
Яркие нейроны с большим количеством цитохрома С оказались у здоровых пожилых людей. У людей с болезнью Паркинсона нейроны окрасились не так ярко. Их митохондрии страдали от дефицита белка и хуже превращали кислород и глюкозу в энергию: у них попросту не хватало оборудования.
Возник новый вопрос: почему в митохондриях людей с болезнью Паркинсона так мало цитохрома С? Ученые предположили: ген митохондрий повредился так неудачно, что они не производят достаточно этого белка. Так и оказалось: информация потерялась, а почему — неизвестно. Поврежденные нейроны с неполным геномом были и у здоровых, и у больных пожилых людей. При Паркинсоне их просто было намного больше, а у здорового молодого человека — не было вовсе.
Как именно здоровье митохондрий влияет на нейроны? Исследовать мозг живого человека сложно, поэтому обратимся к исследованиям на мышах. Но сначала вспомним важную вещь: чтобы синтезировать АТФ, митохондрии добывают энергию из кислорода и еды. Но не вся эта энергия идет на синтез АТФ. Часть митохондрии тратят на обогрев тела, часть — на образование активных форм кислорода. А чтобы рассеивать энергию в виде тепла и согреть тело, у митохондрий есть специальные белки.
С этими белками и поиграли ученые, создав мышей с дефектами: одни не могли эффективно синтезировать белки для рассеивания тепла, другие — наоборот, синтезировали их больше обычного. Митохондрии мышей с недостатком белков-энергоотводов производили больше активных форм кислорода: энергии просто некуда было деться. У этих мышей еще и было меньше митохондрий в нейронах. То есть нейроны получали и больше вреда, и меньше энергии. Потом ученые использовали на мышах нейротоксин, который вызывает гибель нейронов и Паркинсон. Мыши с недостатком белков заболевали гораздо быстрее.
Митохондрии и иммунитет
Бактерия слилась с клеткой, стала производить для нее энергию — и стала митохондрией. Скорее всего, изначально эта бактерия обеспечивала хозяина еще и защитой. Активные формы кислорода она использовала, чтобы разрушить и переварить захваченные клеткой патогены — бактерии или вирусы. Возможно, именно это сотрудничество стало нашей иммунной системой.
Сейчас митохондрии помогают организму быстро и эффективно реагировать на травмы. Когда клетки повреждаются, высвобождается митохондриальная ДНК — и попадает в кровь. Митохондриальная ДНК похожа на бактериальную, поэтому организм считывает это как сигнал опасности и активирует иммунный ответ.
А еще митохондрии активируют иммунные клетки. Например — макрофаги. Когда макрофаги получают от организма сигнал, что в тело проник патоген, митохондрии макрофагов переквалифицируются из энергостанций в военные сооружения. Они перестают синтезировать АТФ и полностью переходят на синтез активных форм кислорода. Активные формы кислорода, во-первых, говорят организму, что самое время начать сражение с патогеном, а во-вторых, и сами могут его уничтожить.
Митохондрии активны и в Т-клетках. Это спецагенты иммунитета, которые проверяют другие клетки на наличие вирусов, а если находят заболевшие — уничтожают. Как и другие митохондрии, митохондрии Т-клеток сливаются друг с другом и, наоборот, разделяются, меняют форму и размер, чтобы адаптировать процесс производства энергии к состоянию организма. Когда все спокойно, они длинные: это помогает эффективнее работать и производить меньше активных форм кислорода. Но когда организм идентифицирует угрозу (это может быть физическая травма, например), митохондрии Т-клеток фрагментируются — и в крови становится много коротких сегментов митохондриальной ДНК. В таком состоянии митохондрии образуют больше активных форм кислорода и тем самым дают иммунитету понять, что пора действовать.
Митохондрии и психика
Когда мышь испытывает психологический стресс, ее Т-клетки активируются, а митохондрии фрагментируются так же, как если бы ее организм столкнулся с вирусом. Если же создать таких мышей, Т-клетки которых всегда активны, а митохондрии — фрагментированы, они будут тревожными, заторможенными, нелюбопытными и лишенными всякой мотивации. А это уже классическая депрессивная симптоматика. Что ставит перед учеными новый вопрос: что, если митохондрии виноваты в проблемах с настроением у человека?
Чтобы проверить гипотезу, исследователи заставили крыс конкурировать за социальную иерархию. Доминирующие позиции заняли животные с меньшим уровнем тревожности. Потом ученые изучили митохондрии прилежащего ядра мозга крыс — отдела, который регулирует эмоции и поведение что у грызунов, что у людей. Оказалось, у крыс-аутсайдеров митохондрии функционируют хуже. А еще в них меньше белков для превращения кислорода и глюкозы в энергию — то есть не хватает оборудования, чтобы митохондрия работала эффективно. Различие оказалось врожденным.
Неизвестно, делают ли нас, людей, тревожными и депрессивными врожденные особенности митохондрий так же, как и грызунов. Но на стресс митохондрии человека реагируют тем же образом. В одном эксперименте, например, людей подвергли стрессу: обвинили в краже или нарушении ПДД — и заставили за две минуты продумать стратегию защиты. В крови участников увеличилось количество митохондриальной ДНК, которая активировала иммунную реакцию, — совсем как в случае с мышами.
Как оценить состояние митохондрий?
Надежного и доступного не-ученым теста для оценки состояния митохондрий пока нет, хотя изобрести его исследователи пытаются. По словам биолога-физиолога, научного сотрудника Университета 2035 Екатерины Зворыкиной, все же есть два метода, которые позволяют примерно понять, насколько корректно они работают.
I. Эргоспирометрия
Простой способ оценить функциональность митохондрий — эргоспирометрия, которую регулярно делают спортсмены. До и во время выполнения физической нагрузки у человека регистрируют ЭКГ и отслеживают потребление кислорода. Человек бежит по беговой дорожке, а параллельно происходит анализ газообмена. Потом данные сравнивают с состоянием покоя и выводят коэффициент. Если показатель не соответствует норме, это может говорить о перетренированности. А перетренированность — косвенный признак, что митохондрии в плохом состоянии.
Информация полезна тем, кто много и усиленно тренируется. Остальным вряд ли стоит делать тест. Если результат плохой, это может говорить о развитии рака и ряда хронических заболеваний, но для их мониторинга есть и более удобные чекапы.
II. Биохимические тесты
Более точный метод — анализ биохимических маркеров. Помогут следующие тесты.
- Анализ крови на метаболиты: пируват и лактат. Именно пируват митохондрия использует, чтобы синтезировать АТФ. Собственно, этот метаболит образуется как промежуточный этап в цепи реакций, которые превращают глюкозу в энергию. Повышенное содержание пирувата в крови может говорить, что процесс переработки пирувата нарушен, а вместе с ним
— и работа митохондрий.
Лактат — еще один метаболит, который рассказывает о состоянии митохондрий. Наши клетки могут обеспечить себя энергией и без помощи митохондрий — из глюкозы. Но это не так эффективно. Из одной молекулы глюкозы митохондрия вырабатывает 30-32 молекулы АТФ, а клетка без помощи митохондрии — только 2 молекулы АТФ. Поэтому клетка добывает энергию сама, только если кислорода для митохондрий не хватает. Например, во время интенсивных тренировок, когда мышцам не хватает кислорода. А указывает на это повышение содержания лактата. Измерение его уровня используют спортсмены, чтобы подобрать уровень нагрузки и вовремя заметить перетренированность. - Анализ крови и мочи на аминокислоты. Как и пируват, аминокислоты участвуют в метаболизме митохондрий и могут быть в этом процессе топливом. С дисфункцией митохондрий может быть связано повышение содержания в крови и моче аланина, глицина, пролина и треонина.
- Анализ на концентрацию карнитина. Попадая в наш организм, жиры распадаются на жирные кислоты. Потом жирные кислоты должны попасть в митохондрии, а для этого им нужен карнитин. Недостаток или избыток карнитина влияет на синтез АТФ, ведь жиры — самый ценный источник энергии для митохондрий. Количественная оценка карнитина в крови может показать, насколько эффективно митохондрии перерабатывают жирные кислоты.
Но важно помнить: биохимические анализы разработаны для диагностики митохондриальных заболеваний, а не для оценки состояния митохондрий здоровых людей. То же повышение уровня лактата может быть маркером перетренированности, а может говорить о самых разных заболеваниях: от митохондриальной дисфункции до ишемической болезни. Интерпретировать результаты анализов нужно с врачом.
Как помочь митохондриям?
Главная причина нездоровья митохондрий — окислительный стресс, когда активных форм кислорода слишком много. Лекарств для митохондрий пока нет. Но помочь им можно, скорректировав образ жизни. Вот главные интервенции, которые советует биохимик и биохакер Екатерина Щербакова, научный сотрудник ФГБНУ «ЦНИИТ» и автор книги «Питание биохакера».
Ограничить калории
Мы едим, чтобы кормить митохондрии. И для них важно, сколько мы едим. Ограничение калорийности — единственная диета, которая безоговорочно увеличивает продолжительность жизни у лабораторных организмов: от дрожжей и мух до грызунов и обезьян. У них снижается уровень воспаления, а аутофагия, естественный процесс избавления от «клеточного мусора», активируется. В том числе активируется митофагия — аутофагия митохондрий, что позволяет удалять неработающие митохондрии.
Одновременно с этим повышается уровень нейротрофического фактора мозга (BDNF), что способствует формированию новых нейронов и синапсов. В результате ограничение калорий замедляет гибель нейронов у животных с болезнями Хантингтона, Альцгеймера, Паркинсона. А еще — снижает частоту возрастных заболеваний: рака, диабета, болезней сердца.
Почему так? Молекулярных бонусов ограничения калорий несколько. Например, оно приводит к восстановлению одного из главных клеточных антиоксидантов — глутатиона, а также уровня кофермента NAD+, который помогает превращать питательные вещества в энергию. А еще голод активирует сиртуины. Эти белки имеют две функции. Во-первых, выключают гены, использовать которые клетка в режиме голода не должна. Во-вторых, участвуют в устранении повреждений ДНК, в том числе — вызванных активными формами кислорода.
Морить себя голодом ради здоровья митохондрий не нужно. Достаточно урезать суточную калорийность рациона на 25%. Так сделали в одном американском исследовании со здоровыми людьми с лишним весом. Женщины, например, вместо 2200 ккал съедали 1650 ккал — что меньше нормы, но не настолько, чтобы мучиться от голода. Через шесть месяцев у участников эксперимента уменьшилось повреждение митохондриальной ДНК. Митохондрий стало больше, и они стали эффективнее функционировать. Похожие эффекты ученые наблюдают и у мышей при интервальном голодании.
Почему голод помогает митохондриям? С точки зрения организма, клетка в бедственном положении. Она бросает все силы на производство энергии. При этом активируются ферменты антиоксидантной защиты, репарации. В результате увеличивается и количество, и работоспособность митохондрий.
Кормить митохондрии витаминами и антиоксидантами
Просто ограничить калории недостаточно. Митохондрии нуждаются в витаминах, микроэлементах и антиоксидантах.
- Витамины группы В нужны митохондриям для работы белков, связанных с производством АТФ. Если питаться разнообразно и есть мало переработанных продуктов и много цельных, этих витаминов в организме будет достаточно.
- Коэнзим Q10 незаменим в процессе синтеза АТФ. Природные источники — мясо, рыба.
- Кверцетин также помогает митохондриям: это природный антиоксидант, который нейтрализует активные формы кислорода. Исследование на человеческой клеточной линии показало, что он повышает биогенез митохондрий внутри клеток — то есть в клетке их становится больше. Ищите кверцетин в красном луке, укропе и ягодах.
- Ресвератрол (тот самый антиоксидант, который якобы делает полезными вино и шоколад) продлевает жизнь дрожжам, червям и мухам. При этом он активирует сиртуин — белок, который делает полезным ограничение калорий. Из-за этого ресвератрол даже называют «миметиком голода»: в организме он включает те же механизмы, что активируются при голодании. Еще ресвератрол усиливает биогенез митохондрий. Лучше ищите его в винограде, чернике и арахисе, а не в вине и шоколаде.
Подкармливать кишечные бактерии гранатом и орехами
В кишечнике человека живет множество бактерий. Среди них есть союзники, которые помогают иммунной системе распознавать патогены. Эти кишечные бактерии общаются не только с иммунными клетками, но и с митохондриями.
Странно ли это? Вовсе нет, если вспомнить о бактериальном происхождении митохондрий. Общаются митохондрии и бактерии на языке метаболитов. Например, бактерии выделяют короткоцепочечные жирные кислоты, которые нужны митохондриям для синтеза АТФ. Или уролитин А — вещество, которое активирует митофагию — процесс уничтожения дефектных митохондрий, которые уже производят не энергию, а активные формы кислорода.
Уролитин А синтезируют бактерии Eggerthellaceae. Они используют для этого вещества, которые есть во фруктах и ягодах (гранат, малина) и орехах (идеальный вариант — грецкий). А еще для Eggerthellaceae и для других кишечных союзников полезны клетчатка, ферментированная пища, пробиотики и пребиотики.
Больше двигаться
Самый эффективный способ улучшить работу митохондрий — регулярные тренировки: они увеличивают и количество, и качество митохондрий. Так происходит потому, что сокращение мышц — процесс энергозатратный. Сами по себе мышцы не сокращаются. Чтобы их стимулировать, организм использует АТФ. А АТФ синтезируют митохондрии. Потому стоит нам начать двигаться, как клетки адаптируются, чтобы получать больше АТФ: ведь она теперь активнее тратится.
Мышечные клетки ускоряют работу своих митохондрий: синтезируют белки, необходимые для расщепления жирных кислот, — и отправляют их в митохондрии. Митохондрии получают больше белков, расщепляют жиры быстрее, используют больше кислорода и глюкозы — и синтезируют больше АТФ. Параллельно мышечные клетки запускают процесс биогенеза митохондрий. Митохондрий в клетке становится больше — и мы получаем больше АТФ.
Но и это еще не все. Когда мы занимаемся спортом, клетка остро нуждается в АТФ и поднимает планку для митохондрий. Чтобы отсеять плохо работающие органеллы, она активно синтезирует специальные белки, которые проверяют, насколько хорошо те работают. Если белки обнаруживают, что митохондрия работает так себе, клетка ее уничтожает. Иными словами, когда мы активно двигаемся, мы избавляемся от дефектных митохондрий.
Тренироваться разнообразно
Различные типы тренировок воздействуют на различные типы мышечных волокон — и по-разному влияют на митохондрии. Обычно советуют аэробные тренировки: одного упражнения на выносливость уже достаточно, чтобы митохондрии стали работать немного эффективнее. При длительных тренировках объем митохондрий обычно увеличивается на 40–50%, и это происходит параллельно с улучшением работы митохондрий.
Но аэробные тренировки бывают разными — и по-разному влияют на мышцы и митохондрии. Продолжительные кардионагрузки вроде длительного бега, плавания и езды на велосипеде задействуют в первую очередь медленные мышечные волокна и митохондрии в них. Для адаптации митохондрий в красных мышечных и белых мышечных волокнах нужна высокоинтенсивная, но короткая тренировка. Например, интервальная тренировка спринта (SIT) или интервальная тренировка высокой интенсивности (HIIT) — они сочетают и аэробную, и анаэробную нагрузку.
А вот польза чисто анаэробных тренировок для митохондрий — вопрос спорный. Раньше считалось, что силовые тренировки не так хороши, как кардио: они увеличивают объем мышц, но не меняют качество самих мышечных клеток, а значит, не влияют на работу митохондрий. Но появляются новые данные, согласно которым упражнения с отягощениями стимулируют биогенез митохондрий в мышцах и производство митохондриями энергии [1, 2]. Так что самое практичное решение — сочетать разные типы нагрузки: и бегать на длинные дистанции, и делать интервальные тренировки высокой интенсивности, и не забывать про силовые тренировки.
Не забывать отдыхать
Спорт для митохондрий полезен, но не когда его слишком много. Если перестараться, можно повредить мышечные клетки, что приведет к их атрофии и синдрому перетренированности. А еще изнурительные тренировки стимулируют повышенное образование активных форм кислорода, что вредит митохондриям.
Также по теме. Микробиом: как полюбить полчища населяющих нас бактерий. Ссылка.
Claude помог пользователю вернуть утерянные 11 лет назад биткоины
Сейчас они стоят порядка $400 000
Витамин D: пить или не пить летом 2026 года?
Крупнейшая эндокринологическая организация мира пересмотрела рекомендации по приему витамина. Разбираемся, когда, кому и сколько стоит его принимать